M1 STIS
Sciences, Techniques et ingénierie de la santé
Navigation :
NF KappaB : Suppresseur de tumeur ou oncogène ?
Réponse cellulaire à l'oncogène Ras
Membrane et récepteur Fas dans l’apoptose induite par le cisplatine
Régulation du gène suppresseur de tumeur p53
- Les protéines de la famille p53
- Les protéines de la famille ASPP
- Régulation de p53 par les protéines de la famille ASPP
Nouveaux composants dans la signalisation de la maladie de Parkinson
Liens externes :
Rôle des caractéristiques membranaires et du récepteur de mort Fas dans l’apoptose induite par le cisplatine
I Présentation générale
Formation d’adduits à l’ADN :
L’action principale et la plus connue du cisplatine est l’induction de l’apoptose par la formation d’adduits à l’ADN. Cette induction est possible car le cisplatine peut interagir avec l’ADN via le site nucléophile N7 des bases puriques. Il peut ainsi former des complexes ADN/protéine ou ADN/ADN inter et intra-chaînes. La forme majeure obtenue est la forme intra-chaînes qui représente 85-90% des adduits (Kelland, 1993) et il a été montré qu’il existe une relation linéaire entre la quantité de platine liée à l’ADN et la cytotoxicité (Fraval et Roberts, 1979 ; Roberts et Fraval, 1980).
Ces adduits induisent des distorsions de l’ADN qui permettent la fixation de nombreuses protéines de reconnaissance dont des protéines de réparation de l’ADN mais également des protéines induisant l’apoptose (Donahue et al., 1990 ; Fink et al., 1998 ; Chaney et Vaisman, 1999). Parmi les protéines de reconnaissance se trouvent :
- hMSH2 qui appartient au complexe MMR qui permet la réparation de l’ADN.
- HMG1 et HMG2 qui régulent localement, avec l’histone H1, la condensation de la chromatine. HMG1 aurait un rôle cytotoxique par interaction avec l’adduit en inhibant sa réparation.
- hUBF qui se lie à l’élément en amont UCE et permet le recrutement de l’ARN polymérase I.
- TBP qui se lie à la TATA box et permet le recrutement de l’ARN polymérase.
Ces deux dernières protéines seraient séquestrées par l’adduit ce qui empêcherait ainsi leur participation à la transcription. Il est intéressant de noter que MMR et HMG1 sont plus spécifiques des adduits formés par le cisplatine que par d’autres analogues tels que le JM216 ou l’oxaliplatine (Fink et al., 1996 ; Chaney et Vaisman, 1999 ; Zdraveski et al., 2002).
L’induction d’adduits par le cisplatine induirait l’arrêt transitoire de la phase S suivit d’un blocage des cellules en G2/M. Ce blocage est induit par l’inhibition du complexe cdc2-cycline A ou B. Les adduits inhiberaient aussi la phase G1 probablement via p16INK4A qui est un inhibiteur du complexe cycline D/cdk4 (Shapiro et al., 1998). L’arrêt du cycle est nécessaire pour permettre l’excision et la réparation de l’ADN endommagé. Si la réparation est complète la cellule survie. Dans le cas contraire, lorsque les dommages sont trop importants, l’apoptose est induite.
Se pose alors la question du rôle de la protéine majeure de l’apoptose, à savoir p53.
Rôles de p53 :
Il a été montré que p53 est induite et activée en présence de cisplatine et que cette activation est dépendante de la voie des MAP kinases et d’ATR. Il s’agit d’une kinase préférentiellement induite par le cisplatine qui a été décrite comme étant associée à la voie des MAPK. Elle permet la phosphorylation de p53 sur de nombreuses positions telles que la Sérine 15, la Thréonine 81 ou la Sérine 20 lorsqu’elle active la kinase CHK1 (Persons et al., 2001 ; Appella et Anderson, 2001 ; Shieh et al.,2000). La sous famille majeure des MAPK est constituée de ERK, des JNK et de p38 et régule la prolifération, la division, la survie cellulaire et l’apoptose. Ces protéines sont induites par le cisplatine et en particulier ERK qui est la plus importante dans l’induction de l’apoptose via le cisplatine en activant p53 par régulation de sa phosphorylation sur la Sérine 15 (Wang et al., 2000 ; Persons et al., 2000). L’induction et l’activation de p53 est nécessaire pour son activité de facteur de transcription.
Le lien entre la reconnaissance des adduits de l’ADN, produits par le cisplatine, et l’activation de p53 passerait également par les protéines HMG1 et HMG2 qui augmenterait sa capacité de fixation à l’ADN. Le cisplatine induit donc, via p53, l’activation de nombreux gène et en particulier des gènes d’arrêt du cycle cellulaire, de réparation de l’ADN ou de l’apoptose. Parmi ces gènes on retrouve p21, qui est un inhibiteur des complexes cyclines/cdk, mais aussi gadd45a et Bax ( Delmastro et al., 1997 ; Hershberger et al., 2002). Gadd45a permet la protection des cellules contre les dommages de l’ADN tant que les dommages ne dépassent pas un certain seuil.
Dans le cas contraire se met en place un mécanisme complexe qui commence par la translocation de Bax dans la mitochondrie. Cette relocalisation induit une cascade d’évènements, en particulier la libération de cytochrome C ainsi que l’activation de la voie caspase 9-caspase 3, conduisant à l’apoptose (Wang et al., 2000 ; Makin et al., 2001). Ce mécanisme est finement régulé par la balance Bax/Bcl-2 : quand Bax est induit par le cisplatine le ratio bascule en faveur de l’apoptose. Le cisplatine présente également la capacité de cliver Bcl-2 en un produit Bax-like (del Bello et al., 2001).
L’apoptose induite par le cisplatine peut également être induite par p53 via le récepteur de mort Fas. Il engendre l’activation de la voie caspase 8-caspase 3. Cette voie n’implique cependant pas la mitochondrie et reste assez méconnue (Micheau et al., 1997 ; Muller et al., 1998).
p73 semble aussi pouvoir médier l’apoptose via c-Abl et le complexe MMR qui reconnaît les dommages de l’ADN.
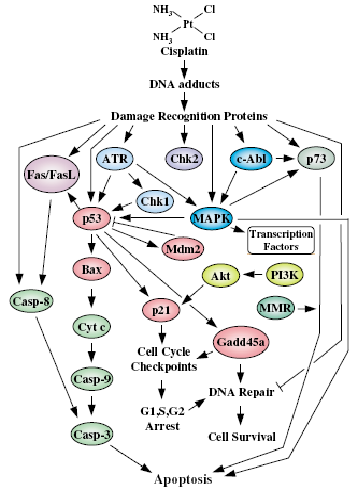
L’ensemble de ses voies d’induction de l’apoptose et en particulier le rôle central de p53 et de p73, sont résumées sur la Figure 1.
Cependant les effets des adduits de l’ADN sur p53 et sur l’apoptose sont insuffisants pour expliquer la grande cytotoxicité du cisplatine. La membrane plasmique joue donc sûrement un rôle dans l’apoptose induite par le cisplatine.
Membrane plasmique :
Nous ne décrirons pas ici les mécanismes à proprement parlé de l’apoptose liée à la membrane plasmique. Ils seront détaillés dans la seconde partie du rapport. Nous détaillerons ici un à un les différents éléments cellulaires impliqués dans cette apoptose.
La membrane plasmique est un élément très important dans tout ce qui concerne les contacts avec la cellule. Elle offre une protection contre l’environnement, mais laisse aussi la cellule communiquer avec celui-ci. Il y a formation de radeaux lipidiques sous l’influence de lipides comme le cholestérol et GM1 qui stabilisent la membrane. Ces radeaux permettent le regroupement en structure ordonnée d’acteurs de voie de signalisation, qui permettent soit la transmission d’un message vers l’extérieur de la cellule, soit la transduction d’un signal extérieur vers l’intérieur de la cellule.
Les radeaux lipidiques ne sont pas tous constitutifs de la membrane, en effet, certaines voies ne sont activées qu’occasionnellement ou à une période de vie de la cellule.
La fluidité membranaire est caractérisée par le paramètre S, qui est le paramètre d’ordre de la membrane, et qui permet d’évaluer la taux d’organisation de la membrane (Rebillard et al., 2007).
Les radeaux lipidiques sont donc des structures dynamiques, rassemblant protéines et lipides, et flottant sur la membrane. Ils peuvent former de grandes plateformes organisées, enrichies en cholestérol, sphingomyéline et glycosphingolipides (Lacour et al., 2004).
Echangeur sodium-proton NHE1 :
L’apoptose induite par le cisplatine entraîne une acidification intracellulaire due à l’inhibition du canal NHE1. Le canal NHE1 est un canal situé sur la membrane plasmique des cellules rénales et intestinales. C’est un antiport composé de 815 acides aminés qui est impliqué dans la régulation du pH pour éliminer les acides générés par le métabolisme actif ou pour répondre aux conditions hostiles de l’environnement.
La sortie d’un proton est accompagnée de l’entrée d’un ion sodium selon le gradient chimique. Cet échangeur joue un rôle important dans la transduction du signal.
La sphingomyélinase acide :
La sphingomyélinase acide est une enzyme de 620 acides aminés qui convertit la sphingomyéline en céramide. Elle est localisée dans le cytoplasme lorsqu’elle est inactive sur les membranes des lysosomes. Sa phosphorylation par PP2A (céramide activated Ser/thr phosphatase) permet sa relocalisation sur le feuillet externe de la membrane plasmique, où elle réduit la sphingomyéline. L’activité de cette enzyme est médiée par différents activateurs, comme des récepteurs proapoptotiques tels que Fas et TNF-R (Tumor Necrosis Factor Receptor), des stress tels que l’irradiation aux UV et des agents antiprolifératifs comme le rituximab (Rebillard et al., 2008).
Le cytosquelette :
L’activation de l’apoptose entraîne des modifications du cytosquelette. Le cytosquelette est composé de protéines qui polymérisent et forment de longs filaments tels que les microtubules, les neurofilaments et les microfilaments, qui confèrent ainsi aux cellules une forme particulière. Ces filaments sont entres autres composés d’actine et nécessitent des points d’ancrage à la membrane. Les protéines ERM (Ezrin, Radixin Moesin) sont des protéines qui interviennent dans ce type de liaison et qui interagissent également avec les radeaux lipidiques (Hébert et al., 2008).
L’ezrine est une protéine constituée de 586 acides aminés qui sous sa forme active va se lier à l’actine et ainsi promouvoir la formation de lamellipodia et de filopodia, qui sont des structures cellulaires. La forme inactive de l’ezrine est localisée dans le cytoplasme, puis elle est relocalisée à la membrane grâce à deux événements : sa liaison au PIP2 (Phosphatidyl Inositol Biphosphate) en son extrémité amino-terminale et sa phosphorylation sur la thréonine 567 en carboxy-terminal. La structure tridimensionnelle particulière dans sa forme inactive bloque le site de liaison à l’actine par un repliement de C-ter sur N-ter. Le PIP2 et la phosphorylation permettent le dépliement de la protéine et son interaction avec l’actine pour la formation de structures essentielles pour la motilité et le contact de la cellule avec d’autres types cellulaires (Zeidan et al., 2008).
Le récepteur de mort Fas :
Fas est une protéine membranaire de 45kDa qui appartient à la famille des Tumors Necrosis Factor (TNF). Son activation permet son agrégation et sa liaison à son ligand naturel, Fas ligand (Fas-L), protéine de la même famille qui existe sous deux formes, l’une secrétée de 26kDa, la seconde membranaire de 40kDa. L’agrégation du récepteur Fas et son activation permettent d’activer une voie principale qui implique Fas Associated Death Domain (FADD) et qui connecte les récepteurs à la cascade des caspases. Ainsi, la supposée première protéine de cette cascade, la procaspase 8 est activée.