M1 STIS
Sciences, Techniques et ingénierie de la santé
Navigation :
NF KappaB : Suppresseur de tumeur ou oncogène ?
Réponse cellulaire à l'oncogène Ras
Membrane et récepteur Fas dans l’apoptose induite par le cisplatine
Régulation du gène suppresseur de tumeur p53
- Les protéines de la famille p53
- Les protéines de la famille ASPP
- Régulation de p53 par les protéines de la famille ASPP
Nouveaux composants dans la signalisation de la maladie de Parkinson
Liens externes :
Régulation du gène suppresseur de tumeur p53
I Les protéines de la famille p53
Présentation :
Historique
| 1979 | découverte de la protéine p53 par quatre équipes de recherche. Trois équipes vont montrer que p53 est capable d’intéragir avec des protéines exprimées par des virus cancérigènes, l’antigène T du virus SV40. L’autre équipe, caractérise p53 en regardant ce qu’induit un traitement tératogène sur le contenu en protéine du sérum de souris. Ils observent alors une augmentation d’une protéine de 53kDa. Il faudra attendre 1985 pour comprendre que cette équipe avait mis en évidence la même protéine que les trois autres. |
|---|---|
| 1983 | mise en évidence que l’injection intracellulaire d’un anticorps anti-p53 bloque le cycle cellulaire. p53 est alors qualifié d’oncogène. |
| 1985 | le gène de p53 humain est cloné, ce qui permet de remarquer que les quatres équipes avaient isolé la même protéine en 1979. |
| De 1985 à 1989 | l’étude des propriétés de la protéine conduit à la classer parmi les oncogènes, ce qui signifie qu’elle permet le développement tumoral. |
| 1988 | mise en évidence que les gènes étudiés jusqu’alors sont mutés. La protéine « sauvage » a des effets totalement opposés, et p53 serait donc un gène suppresseur de tumeurs. |
| 1989 | deux équipes américaines (celle de Voglestein et celle de Minna) découvrent que p53 est rendue inactive par mutation dans un grand nombre de cancers humains. |
| De 1989 à nos jours | la protéine p53 est considérées comme étant au cœur du développement tumoral et le nombre de laboratoire participant à son étude à considérablement augmenté. |
Structure du gène
La protéine p53 est un facteur de transcription intervenant dans le maintien de l’intégrité du matériel génétique de la cellule. Elle est codée par un gène situé sur le bras court du chromosome 17 (locus 17p13.1) chez l’Homme. Il est situé sur d’autres chromosomes pour d’autres espèces (chromosome 11 chez la souris et 5 chez le chien par exemple).
Il s’agit d’un gène d’environ 22kpb, comprenant onze exons et dix introns. La transcription de ce gène donne un ARNm de 2,2kb qui sera ensuite exporté dans le noyau pour être traduit à partir d’un codon ATG situé dans l’exon 2. Dans la forme dite « sauvage » de la protéine, l’exon 9 n’est pas traduit.
Structure de la protéine
La protéine p53 est une protéine de 393 résidus d’acides aminés lui conférant une masse moléculaire d’environ 53kDa. Elle a pu être détectée au niveau du noyau de la cellule, du cytoplasme et du réticulum endoplasmique. Des études ont également montré une localisation à la membrane de la mitochondrie, permettant une activation directe de protéines telles que BAX, pour induire l’apoptose.
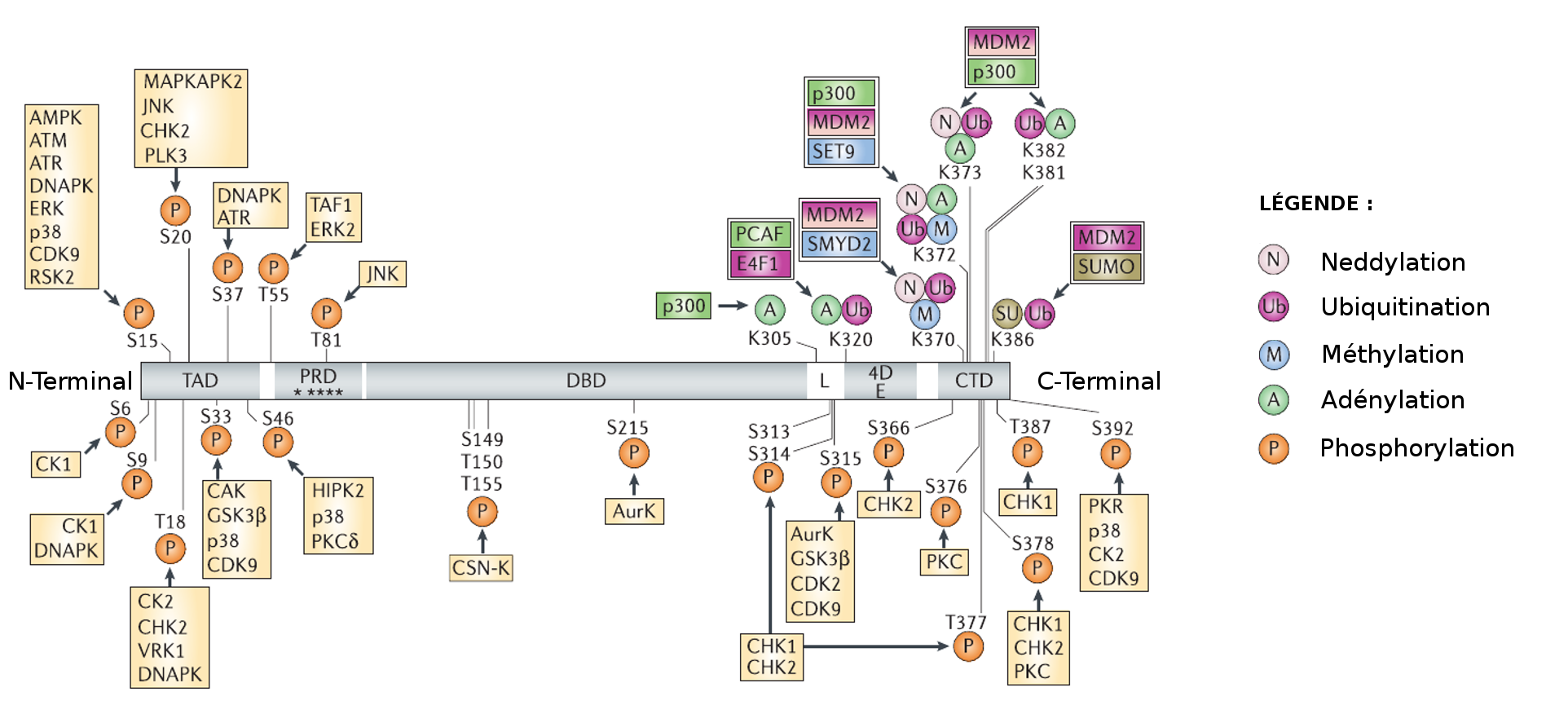
Comme le montre la figure 1, elle est organisée en plusieurs domaines, avec un domaine de transactivation (TAD) à l’extrémité amino terminale, suivi d’un domaine riche en proline (PRD), d’un large domaine de fixation à l’ADN (DBD), d’une séquence intervenant dans la tétramérisation (4D), et une séquence régulatrice contenant le signal de localisation nuclaire (CTD) en C-terminal.
On peut noter que les mutations affectant la protéine ont, pour la grande majorité, été mises en évidence dans le domaine de fixation à l’ADN. Ainsi, la protéine perd sa capacité de liaison avec l’ADN, et ne permet plus la synthèse de protéines de réponse aux stress cellulaires.
p53, p63 et p73 : une famille de protéines
Il a récemment été mis en évidence le fait que p53 avait une homologie structurale avec deux autres protéines que sont p63 et p73. Cette homologie aurait tendance à suggérer que ces trois protéines aient des fonctions biologiques proches. Pourtant, la réalisation de souris knock-out pour p53 donne des souris ayant un phénotype normal mais développant des tumeurs de façon spontannée. Les souris knock-out pour p63 montrent une mortalité post-natale, une dysplasie ectodermique, un palais fendu, et des défauts de formation des membres. Enfin, les souris dont le gène de p73 a été inactivé affichent des défauts de la neurogénèse. De plus, les protéines p63 et p73 sont très peu mutées dans les cancers humains.
p53 est une protéine qui répond aux stimili génotoxiques alors que les deux autres protéines semblent intervenir dans le développement et la différenciation tissulaire. Pourtant, malgré ces différences, ces trois protéines semblent coopérer lors de la réponse à un génotoxique.
p53 : un gène suppresseur de tumeurs
Selon l’hypothèse de Knudson, un gène suppresseur de tumeur est un gène qui, lorqu’il est inactivé sur ses deux allèles, induit le développement tumoral. L’une des deux inactivations par mutation peut être héritée d’un des deux parents.
La protéine p53 répond à cette définition puisque la réalisation de souris knock-out pour p53 montre que les animaux ont tendance à développer des tumeurs de façon spontanée. Lorsqu’elle est inactivée dans les tumeurs, elle ne peut plus jouer pleinement son rôle de facteur de transcription car une large majorité de mutation touche le domaine de liaison à l’ADN de la protéine. Ainsi, elle ne peut pas induire la transcription puis la traduction de protéines intervenant soit dans la réparation des dommages causés par le stress, soit dans la destruction de la cellule.
p53 est donc une protéine dont le taux de base dans la cellule est relativement faible. Lorsque cette dernière est soumise à un stress, on observe une augmentation du taux de protéines intracellulaires. Le facteur de transcription induit alors la synthèse de protéines impliquées dans l’arrêt du cycle cellulaire, l’apoptose, la sénescence, la réparation de l’ADN ou encore la différenciation. Si aucune de ces issues n’est vérifiée, la cellule entre alors dans des séries de divisions anarchiques correspondant au processus de cancérisation.
Fonctions et régulations
Activation
La protéine p53 est la gardienne de l’intégrité du matériel génétique de la cellule. Elle se trouve être exprimée dans des cellules soumises à un stress et en particulier lors de stress induisant des mutations. Son implication dans la quasi totalité des étapes conduisant au développement tumoral rend son étude particulièrement intéressante mais également extrêmement difficile.
Dans les conditions physiologiques, la protéine p53 est présente en faible quantité dans la cellule. En effet, lors de sa synthèse dans le cytoplasme, elle est tout de suite prise en charge par la protéine mdm2. Cette dernière est une protéine E3 ligase, qui va charger la protéine p53 avec plusieurs chaînes d’ubiquitine, entraînant sa dégradation dans le protéasome (structure protéique cylindrique contenant des protéases et dont la fonction est de dégrader les protéines dans la cellule).
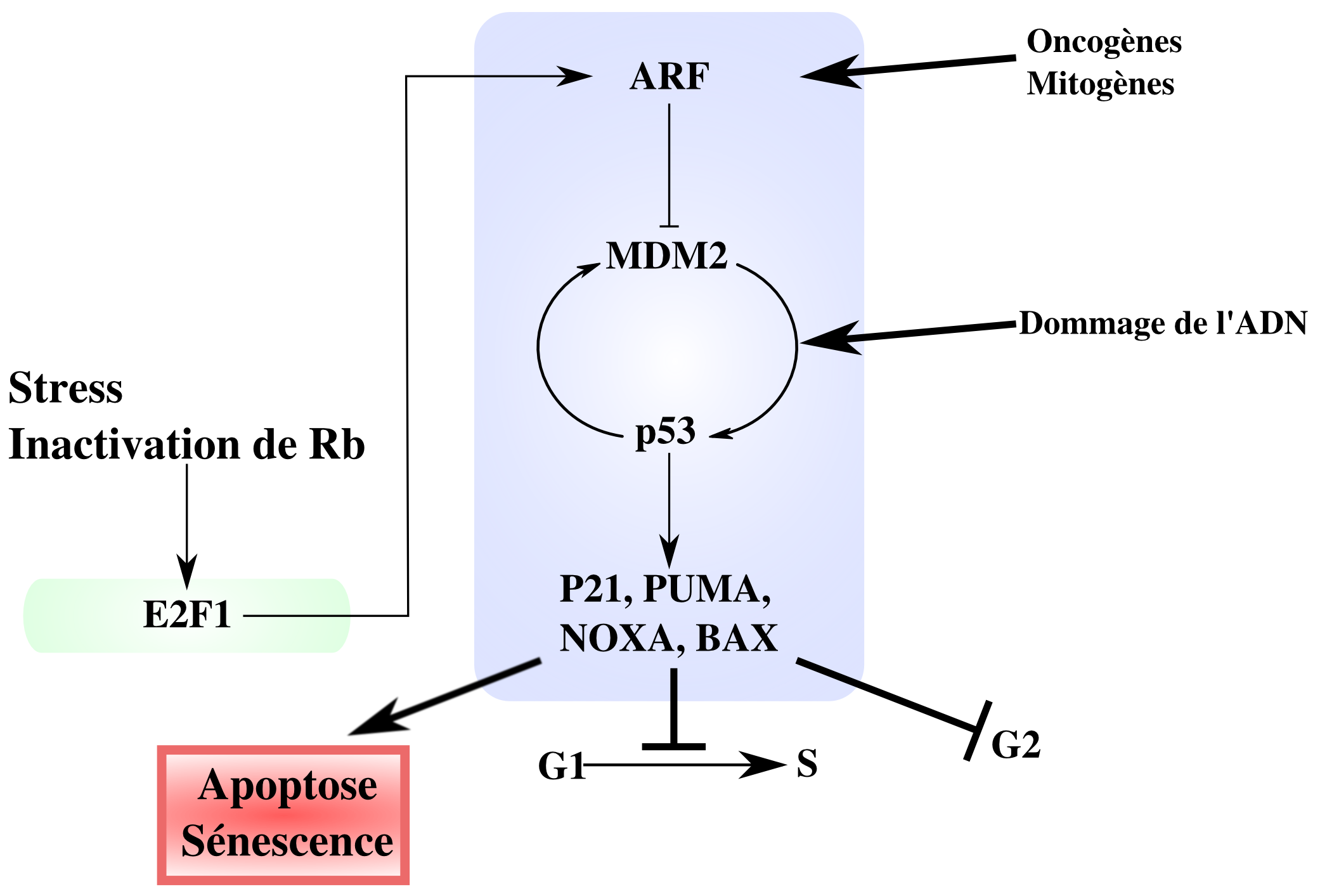
Lors d’un stress, l’association entre p53 et mdm2 est abolie, p53 peut alors migrer dans le noyau. En effet, la cellule stressée exprime fortement le facteur de transcription E2F1. Ce dernier est capable d’induire la synthèse de la protéine ARF qui peut alors dégrader mdm2, permettant ainsi une stabilisation de p53 et l’augmentation de son taux intracellulaire. Comme tout facteur de transcription, p53 peut se fixer à l’ADN pour pouvoir activer les gènes qu’il active ou réprime, tels que p21, bax, puma. . . Pour cela, p53 doit également être acétylée par la protéine CBP1 . Cette acétylation s’effectue sur les lysines en position 320 et 382, et permet d’augmenter la liaison à l’ADN de p53. Elle peut ainsi se lier à l’ADN et permettre à l’ARN polymérase d’être recrutée sur ses gènes cibles.
On notera que les modifications post-traductionnelles détaillées ici sont loin d’être les seules, p53 est une protéine extrêmement régulée et ses modifications post-traductionnelles sont très complexes.
Choix des gènes cibles
Les gènes cibles sont également nombreux et peuvent varier en fonction de plusieurs paramètres. Ainsi, mdm2 est par exemple un des gènes cibles de p53 ce qui permet d’avoir un rétrocontrôle négatif, en particulier dans la cas où la cellule aurait réussi à réparer les dommages dus au stress. Dans ce cas, l’augmentation du taux de p53 permet à la protéine de sortir du cycle cellulaire afin de réparer les atteintes, et la dégradation de p53 par mdm2 permet un retour à la normale avec la reprise du cycle cellulaire. Les gènes cibles de p53 peuvent cependant être classés en cinq grands groupes car ils interviennent dans cinq types de réponses que sont l’arrêt du cycle cellulaire, la sénescence, l’apoptose, la réparation de l’ADN ou encore la différenciation.
L’orientation de p53 vers les uns ou les autres s’effectue selon un mécanisme encore inconnu. Il semblerait que plusieurs facteurs entrent en jeu et notamment l’affinité de la protéine pour les différents promoteurs, le type de cofacteurs qui lui sont associés, ou encore ses modifications post- traductionnelles. Il est très probable que ces trois éléments concourent à la sélection de tel ou tel type de gènes cibles par p53, permettant ainsi à la cellule de s’orienter vers l’une des cinq voies précédemment citées.